2024年1月9日,卫材和渤健联合开发的阿尔茨海默病(AD)新药仑卡奈单抗(商品名:乐意保/Leqembi)在国内获批上市,用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆。
Leqembi(lecanemab,仑卡奈单抗)是一款靶向脑内β淀粉样蛋白(Aβ)的单克隆抗体,2023年1月,美国FDA加速批准leqembi用于治疗阿尔茨海默病,2023年7月,FDA宣布在确认临床疗效后,将leqembi转为完全批准。
在中国,2023年10月,仑卡奈单抗通过海南省药品监督管理局审核落地海南博鳌乐城国际医疗旅游先行区,定价每瓶3328元,规格 200 毫克(2 毫升)每瓶。按此价格,一个60公斤体重的患者月均治疗费用约2.17万元,年治疗费用约26万元。本次仑卡奈单抗获NMPA批准正式进入中国,据北京日报报道,该药上市后预计定价 2508 元,即一个 60公斤体重的患者月均治疗费用约1.5万元,年治疗费用约18万,较此前便宜了四分之一。如果未来能进入医保,价格有望进一步降低。
图片来源:卫材中国微信公众号
首个针对病因的AD治疗药物
阿尔茨海默病(AD)是一种进行性、不可逆的神经退行性脑疾病,会导致患者智力障碍、精神异常、社会与生活功能丧失,严重影响患者的认知能力和正常生活。
流行病学调查显示,截至2018年,中国60岁以上的人口中,阿尔茨海默病患者有983万人,轻度认知障碍患者有3877万人。而随着我国人口老龄化趋势加快以及主要心血管疾病及相关因素流行趋势增加等多种因素的影响,阿尔茨海默病的患病率和患者数量也呈逐年递增的趋势。据估计,到2050年,阿尔茨海默病患者人数将增至4000万人。
但由于AD发病机制复杂且临床试验审核程序非常严苛,AD新药研发业界公认失败率高,被称为药物研发“死亡谷”。
从全球范围看,2003年NMDA受体抑制剂美金刚获批后,该领域上市的新药寥寥无几,且争议颇多。
2019年,绿谷制药的甘露特钠胶囊(GV-971,商品名:九期一)在中国获批,据研究报道GV-971的机理是靶向脑-肠轴,并通过调节肠道菌群的失衡和减少神经炎症来提高认知能力。但该药不少质疑,且并未在中国以外的市场获批。
在国外,Aβ假说是研究的热点。Aβ蛋白沉积是AD患者的典型病理特征。Aβ是一种淀粉样物质,在正常人的大脑内可以被清除掉。Aβ假说认为,在人脑老化的过程中,由于某些原因导致Aβ分解障碍,这些淀粉样物质变为不溶性淀粉样纤丝,随着不溶性淀粉样纤丝增多,形成弥漫性斑块状,慢慢地Aβ在脑内过度沉积导致神经细胞死亡,导致认知功能受损,从而导致AD。
基于这一假说,制药巨头展开了大量研究。然而,这些试验疗法虽然能够成功降低Aβ水平或者消除大脑中β-淀粉样蛋白的沉积,但是对患者的认知能力的衰退却没有帮助,让β-淀粉样蛋白假说备受质疑。
2012年,强生/辉瑞的单抗药物bapineuzumab在3期临床惨遭失败;
2017年,默沙东研发的小分子药物Verubecestat(MK-8931) 3期临床宣告失败;
2022年,罗氏的Gantenerumab 3期临床研究失败;
2023年,礼来宣布Solanezumab用于治疗阿尔茨海默病患者的3期A4研究未达主要终点和关键次要终点。
2021年6月,卫材/渤健研发的Aducanumab(商品名:Aduhelm)获美国FDA批准,用于治疗早期阿尔茨海默病,成为FDA自2003年以来获批用于治疗阿尔茨海默病的首个新药。但该药自审批时就曾争议不断,甚至有3位FDA咨询委员会专家接连辞职,以示抗议。EMA于2021年12月拒绝批准该药在欧盟上市。而且美国医保机构严格限制了Aduhelm的报销,销售业绩一直惨淡。
Leqembi(lecanemab,仑卡奈单抗)是卫材/渤健研发的第二款Aβ单抗,是一种人源化免疫球蛋白IgG1单克隆抗体,通过直接干预阿尔茨海默病致病元凶,直接拮抗聚集的可溶性和不溶性Aβ,从而减少Aβ斑块。
与Aduhelm结局不同,Leqembi于2023年7月获得FDA完全批准,成为FDA批准的第一种也是目前唯一完全获批的能通过这一作用机制延缓疾病进展、降低认知和功能衰退速度的疗法。该药物目前在美国市场的定价为2.65万美元/年,卫材预计2030年全球销售额达到70亿美元(1万亿日元)。
本次仑卡奈单抗在中国获批,定价约18万/年,与海外价格基本一致,将给国内AD患者带来更多治疗选择。
仑卡奈单抗在中国获批,是基于包括中国在内的全球大型3期研究Clarity AD。在Clarity AD研究中,仑卡奈单抗达到了主要终点和所有关键次要终点,且结果具有统计学意义。该药表现出显著的疗效和良好的安全性,用药3个月即降低Aβ负荷,主要终点18个月时临床痴呆评分总和(CDR-SB1)下降了27%,其他所有的关键次要终点也具有显著性结果。
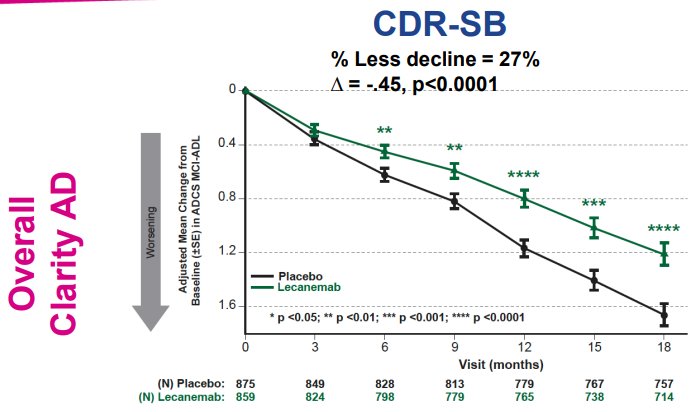
图片来源:卫材官网
更多AD新药有望在未来几年内获批上市
除了仑卡奈单抗,还有多款Aβ及其他机制的阿尔茨海默病在研新药有望在近几年获批上市。
据药智数据,截至2024年1月1日,全球进入临床阶段的阿尔茨海默病药物364个,近三年有更新的有172个,靶向Aβ、微管相关蛋白tau(MAPT)最多。
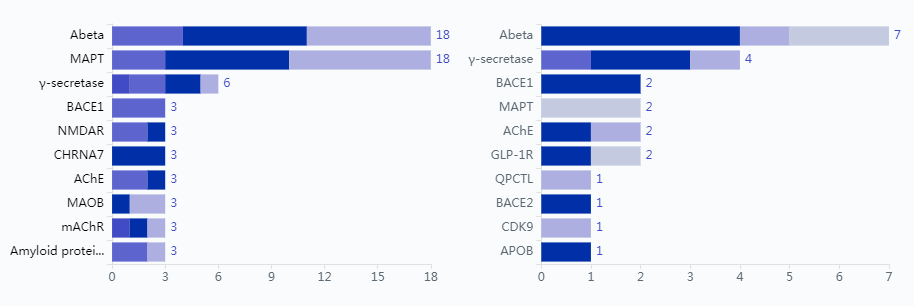
数据来源:药智数据
下面简要介绍其中几款。
礼来:多纳奈单抗(Donanemab)
礼来开发的靶向Aβ淀粉样蛋白药物多纳奈单抗(Donanemab)被认为有超越仑卡奈单抗的潜力。
2023年7,礼来公布了Donanemab的TRAILBLAZER-ALZ 2三期研究的完整结果,显示Donanemab可显著减缓早期症状性阿尔茨海默病(AD)患者的认知和功能下降。主要终点指标(iADRS)显示donanemab延缓了认知功能下降达35%,关键次要终点指标(临床痴呆评分, CDR-SB)显示18个月后donanemab延缓下降36%,数字上看优于仑卡奈单抗的27%。不过两项试验设计不同,不能直接比较。而且多纳单抗的临床试验中有3名患者出现了淀粉样蛋白相关成像异常 (ARIA),随后死亡。目前,礼来已在美国和中国提交多纳奈单抗的新药上市申请并获得受理,很可能成为继仑卡奈单抗之后的第二个Aβ单抗。
恒瑞:SHR-1707
恒瑞团队研发的Aβ单抗是国内首款自研的抗Aβ单抗,于2022年3月进入Ib期临床试验。SHR-1707于2023年阿尔茨海默病协会展示的最新研究结果整体表现符合预期。
除了抗淀粉样蛋白药物,还有很多新机制的在研新药显示出治疗AD的潜力。
礼来:Remternetug
Remternetug是一款下一代N3pG淀粉样蛋白抗体,靶向仅存在于脑淀粉样蛋白斑块中的淀粉样β肽第3个氨基酸的焦谷氨酸修饰,也处于3期临床开发阶段。在2023年AD/PD 会议发布的报告显示,remternetug用以治疗轻度认知功能障碍或轻至中度阿尔茨海默病患者的多中心、随机、双盲1期临床试验取得积极结果,中期分析结果显示remternetug可快速且稳定地清除淀粉样斑块。
渤健/Ionis:BIIB080
BIIB080(IONIS-MAPT)是一款在研反义寡核苷酸(ASO)疗法,旨在靶向微管相关蛋白tau(MAPT)的mRNA以阻止tau蛋白的产生。药物通过与编码tau蛋白的mRNA结合,导致mRNA的降解和tau蛋白水平的下降。
在2023年10月举办的第 16 届阿尔茨海默病临床试验(CTAD)会议上,渤健公布了BIIB080的1b期试验临床积极结果。分析显示,接受该疗法患者展现认知下降改善的趋势。根据此积极结果,渤健已启动相关CELIA临床2期试验。
通化金马:琥珀八氢氨吖啶片
2023年9月,通化金马发布公告称,旗下琥珀八氢氨吖啶片用于治疗轻、中度阿尔茨海默病的3期临床试验已完成揭盲和主要数据的统计分析,达到主要终点达到;在安全性上,试验药物的不良事件及不良反应的发生率均低于两个对照组。琥珀八氢氨吖啶片是一种新的乙酰胆碱酯酶抑制剂,具有双重胆碱酯酶抑制功能,可以同时抑制乙酰胆碱酯酶和丁酰胆碱酯酶。
近两年大热的GLP-1药物不仅在2型糖尿病和肥胖症领域“大杀四方”,在AD领域也显示出治疗潜力。
目前已有研究发现,阿尔茨海默病和2型糖尿病、GLP-1之间存在着千丝万缕的关系,意味着GLP-1也可以在AD领域展现出治疗潜力。
例如,诺和诺德的GLP-1受体激动剂利拉鲁肽,在研究中证明了可以减缓阿尔茨海默病的进展。根据2023年AD/PD国际会议展示的II期ELAD研究结果显示,使用利拉鲁肽可以大大缓解轻度至中度AD疾病进程中出现的大脑萎缩。与安慰剂相比,接受利拉鲁肽治疗的患者大脑的磁共振体积和认知能力下降较慢。
2021年,诺和诺德启动了司美格鲁肽是否能缓解早期阿尔茨海默病患者症状的大型3期试验,初步试验结果预计在2025年产生。
国内药企,天境生物/石药集团的GLP-1 Fc融合蛋白TG103、北京质肽生物的GLP-1受体激动剂ZT002阿尔茨海默病适应症已获得临床试验默示许可。
2023年收获首个上市药物的CRISPR基因编辑,也在阿尔茨海默病领域展现潜力。在2023年阿尔茨海默病协会国际会议上,两项独立的研究探讨了基因如何增加患神经退行性疾病的风险,以及编辑基因如何降低风险或保护大脑免受淀粉样蛋白堆积的影响。
第一项研究来自加州大学圣地亚哥分校的Subhojit Roy实验室。该实验室正在开发一种针对淀粉样蛋白前体蛋白(APP)的基因编辑策略。研究人员发现用CRISPR治疗减少了β淀粉样斑块和相关炎症标志物的数量。他们还看到了神经保护APP产品的增加。而且最重要的是,他们纠正了老鼠的行为和神经系统功能缺陷,且没有在正常小鼠身上观察到任何不良副作用。
另一项研究来自阿姆斯特丹杜克大学教授,其主要候选药物已被发现能在阿尔茨海默病患者的人类诱导多能干细胞衍生的微型大脑和人源化小鼠模型中“显著降低”APOE-e4水平,且不改变其他中性或保护性APOE变体。
AD治疗还有很多挑战
仑卡奈单抗在临床试验中观察到的认知衰退减缓是显著但微小的,并且该药物不会阻止疾病进展。
而且此药的效果也伴随着副作用。超过五分之一的服药患者出现脑肿胀或出血,其余患者没有上述症状,但有时会出现头痛、视力障碍和意识模糊。值得重视的是有五人出现大面积脑出血,三位服用抗凝血药物的患者在试验临床试验期间死亡,刊登在新英格兰杂志的论文显示死亡可能和同时服用抗凝血药物有关。
另外,仑卡奈单抗在美国市场的定价为2.65万美元/年,国内约为18万元/年。
不过仑卡奈单抗的获批仍然可喜可贺,这是自1984年Aβ被确认为AD的独特病理标志后,首个获得多个监管机构认可的新药,让人们看到了攻克阿尔茨海默病的曙光。未来随着更多新兴疗法进入这一领域,攻克阿尔茨海默病也并非不能实现。
文章来源:药智新闻
5858 人阅读过 复制文章链接

推荐文章
-
备孕时不可忽视的问题!
夏秋季节蔬菜瓜果都非常丰富,选择在这个时候 备孕 的 女性 ,能够补充到充足的营养,如果再注意避开一些不利因素,将非常有利于胎宝贝的生长发育。那么,应该注意一些什么呢?
孕前 89人看过 1790点赞

